Neuron(IF 18.688) | 邱照铸研究团队揭示星形胶质细胞GABA释放介导药物成瘾的调控机制
吗啡与可卡因等成瘾药物能激活中脑-边缘多巴胺系统(MLDS),通过不同的细胞机制增加中脑腹侧被盖区(VTA)到腹侧纹状体伏隔核(NAc)的多巴胺信号,从而使个体产生快感,形成药物依赖。目前已知的一种机制是成瘾药物可以抑制VTA GABA神经元的活性从而对DA神经元产生去抑制作用,引起DA神经元活性增强和多巴胺的大量释放,但成瘾药物如何调节VTA GABA神经元活性并驱动成瘾行为仍然知之甚少。2023年1月20日,美国约翰霍普金斯大学邱照铸研究团队在Neuron(IF 18.688)杂志上发表题为“Ventral tegmental area astrocytes modulate cocaine reward by tonically releasing GABA”的研究论文。研究发现可卡因增强VTA中星形胶质细胞GABA的释放,增强VTA GABA神经元的强直性抑制电流,从而抑制VTA中GABA能神经元的电活动,并解除其对DA能神经元的抑制,进而参与成瘾行为。
实验动物
Gad2-Cas9小鼠
(4-6周,电生理实验)
Gad2-Cas9小鼠
(6-8周,行为测试实验)
病毒产品
AAV9-U6-sgGabrd1-U6-sgGabrd2-CAG-FLEX-mCherry
AAV9-U6-sgControl-U6-sgControl-CAG-FLEX-mCherry
使用滴度
1-3x10E12 particles/ml
注射方式
立体定位注射(0.3-0.4μL)
注射部位
VTA(中脑腹侧被盖区)
1. δ-GABAARs介导VTA神经元的强直性抑制
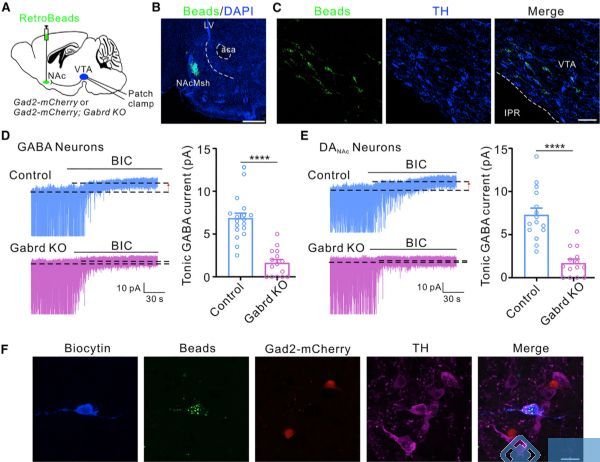
研究表明,包括VTA在内的不同脑区均存在强直性抑制。为了确定强直性抑制在药物成瘾中的作用,作者测量了VTA中GABA和DA能神经元的强直性GABA电流,并标记了投射至NAc区域的DA能神经元(DANAc)。发现在GABAARs(GABA受体)拮抗剂干预的条件下,VTA中GABA和DANAc神经元中观察到相对较小的强直性GABA电流,表明VTA中神经元的强直性抑制与GABAARs相关。δ-GABAARs(δ亚基GABA受体)已被证明在VTA神经元中表达,作者发现δ亚基缺失小鼠VTA中GABA和DANAc神经元的强直性GABA电流显著降低,这表明δ-GABAARs介导VTA神经元的强直性抑制。进一步的研究发现VTA星形胶质细胞中Swell1通道介导GABA释放,并有助于VTA的强直性抑制。
图1. δ-GABAARs介导VTA神经元的强直性抑制
2.可卡因增强了VTA中GABA神经元强直性抑制
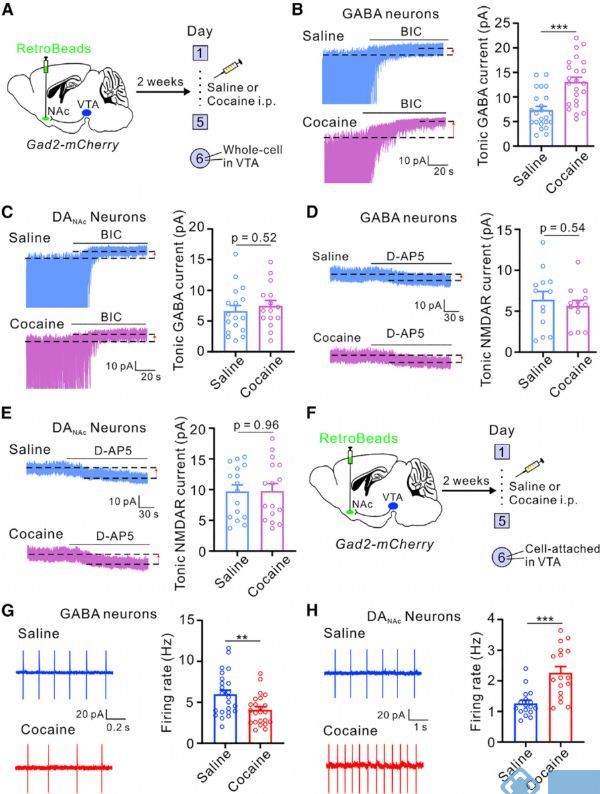
可卡因是一种极易上瘾的药物,作者研究了可卡因对VTA神经元强直性抑制的影响,发现与生理盐水治疗相比,可卡因慢性暴露引起VTA中GABA神经元的强直性GABA电流显著增加,但对DANAc神经元的强直性抑制无影响。此外,与盐水处理的小鼠相比,重复可卡因处理显著降低了VTA GABA神经元的放电频率,但明显提高了DANAc神经元的放电频率,表明对GABA神经元的抑制可能导致了DANAc神经元抑制的解除。之后作者使用THIP(δ-GABAARs的特异性激动剂)验证了这一结论,发现THIP处理降低了VTA GABA神经元的放电频率,但增强了DANAc神经元的放电频率,支持了抑制VTA GABA神经元可以去抑制DANAc神经元的观点。上述这些发现表明可卡因选择性地增强了VTA GABA神经元的强直性抑制,并降低了GABA神经元的放电活动,导致DA神经元的抑制解除。
图2. 可卡因增强VTA GABA神经元的强直性抑制导致DA神经元去抑制
3. 星形胶质细胞Swell1通道介导可卡因诱导的强直性GABA释放和神经元放电变化
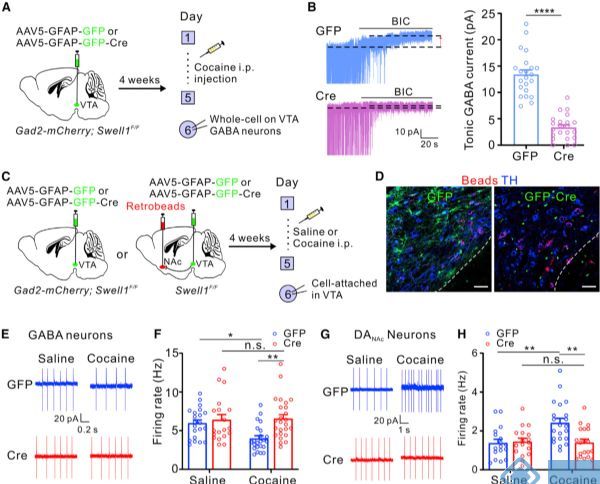
星形胶质细胞Swell1通道在正常情况下介导VTA的强直性抑制,但是否参与可卡因诱发的VTA GABA神经元强直性抑制尚不明确,作者特异性地删除VTA星形胶质细胞中的Swell1,发现可卡因诱发的VTA GABA神经元强直性GABA抑制在Swell1缺失小鼠中被取消,而在对照组小鼠中保持完整。表明星形胶质细胞Swell1参与可卡因诱发的VTA GABA神经元强直性抑制。此外,可卡因暴露抑制了VTA GABA神经元的放电频率,并增加了DANAc神经元的放电频率,但星形胶质细胞Swell1的缺失,消除了可卡因引起的GABA和DANAc神经元放电频率的变化,这表明Swell1介导的强直性抑制在可卡因诱导的VTA神经元活动中起着关键作用。
图3. VTA星形胶质细胞的Swell1缺失消除了可卡因诱导的强直性抑制和神经元变化
篇幅有限,更多文章解读请关注“维真生物”公众号继续阅读~