在我个人看来,对目前做各类分子研究的研究者来说,已有的基础理论其实就是我们所谓的“套路”,沿着这条主干道往下走,就好像去一个山脉寻宝一样,不同的人会选择去不同的山头,寻到的宝自然也不一样,有人毅力大能爬到很高的地方,那里自然宝物更多,因为去的人少。做研究也是一样,如果毅力够大且装备精良,自然能够有更大的机会寻到更为贵重的宝物。前提是—你得沿着主干道去走,当然也有一些人不沿着主干道去走,这样的选择更为艰难和未知,也许会获得一片新的天地,也许会一无所获。
说了这么多,回归主题,今天想带大家看一下同样是lncRNA研究,那些20分的文章是怎么做出来的。下面我们通过一篇lncRNA文章来看一下别人的高分文章都做了些啥?
文章标题:LncRNA GClnc1 Promotes Gastric Carcinogenesis and May Act as a Modular Scaffold of WDR5 and KAT2A Complexes to Specify the Histone Modifi cation Pattern
杂志名称:Cancer Discovery(IF=19.783)
研究方向:医口(胃癌)
基础研究手段:芯片(Arraystar Human LncRNA Microarray V2.0 (8×60KArraystar) 芯片或者测序都无所谓,它们的功能有很大重复性,联川生物可提供相关产品服务)
研究材料:10个胃癌病人的癌症组织和癌旁组织
初步筛选结果:筛选到了8个在癌症和癌旁组织中显著差异表达的lncRNA(芯片信号值大于1500,一般我们要求芯片信号值大于500即可;两倍差异以上以及P值小于0.01)
大量qPCR验证:选取165例癌症和癌旁组织对这8条lncRNA进行验证,发现其中4条lncRNA在胃癌组织中表达量相对癌旁组织显著上升
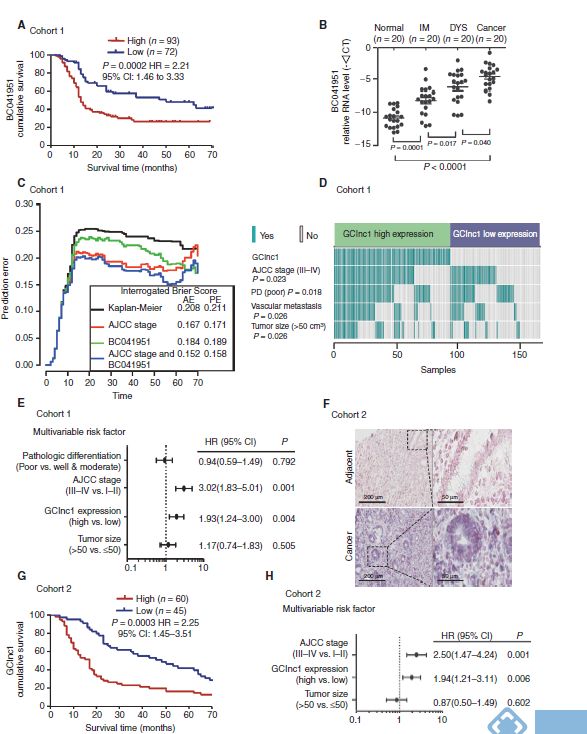
Kaplan–Meier分析:发现只有一条lncRNA的异常表达与胃癌是显著相关的,并且表达量从正常胃组织到胃癌的四个阶段是逐渐增加的。作者因此预测此条lncRNA跟胃癌的发生密切相关,并将其命名为GClnc1。
接下来作者为了验证GClnc1在胃癌中病理学和临床的显著性,做了原位杂交实验,用的是另外105对石蜡包埋的胃癌组织和癌旁组织,发现GClnc1在胃癌组织中的表达量明显比癌旁组织中要高。
接下来为了验证GClnc1是否是一个新的lncRNA序列,作者又使用了Northern blot和5’ RACE以及ChIP对GClnc1进行了验证,并进行了ORF预测,还将细胞质核分离进行qPCR进行验证,最终确定GClnc1是一条新的并且在胃癌组织中高表达的lncRNA。
为了进一步验证GClnc1跟胃癌的关系,作者将GClnc1敲除,再利用RNA-Seq对敲除后的样本进行测序,发现敲除后发生表达差异基因大部分跟胃癌相关,并且,后续的相关功能性实验也证明了GClnc1可以促进癌细胞的增殖和入侵,最终导致胃癌的发生。
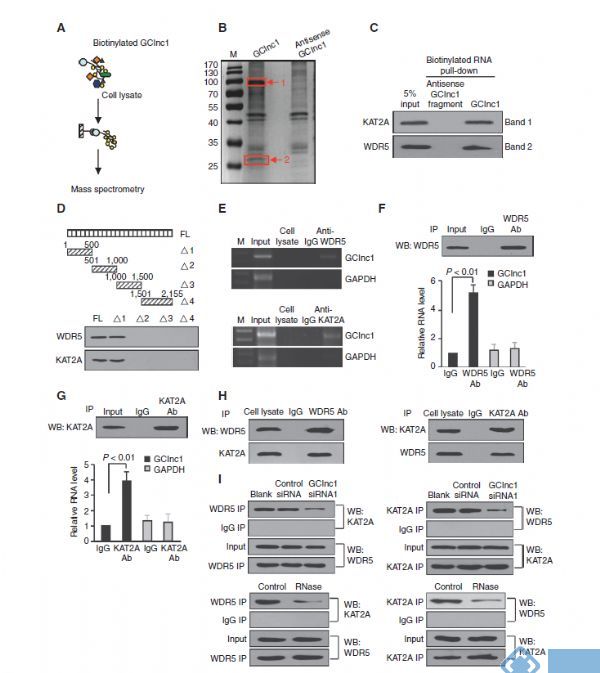
LncRNA研究的套路之一是其可以与转录因子进行结合互作,为了验证GClnc1是否也具有这样的功能,作者利用RNA PULL DOWN实验,利用质谱的方法对PULL下来的蛋白进行鉴定,共鉴定到接近200个蛋白,并且对其中10个跟转录调控的蛋白进行Western blot验证,发现只有WDR5和KAT2A可以和GClnc1特异性结合。且WDR5是H3K4甲基转移酶,而KAT2A是H3K9乙酰转移酶。最后, siRNA和RIP实验证明了GClnc1可与WDR5以及KAT2A结合形成复合物。
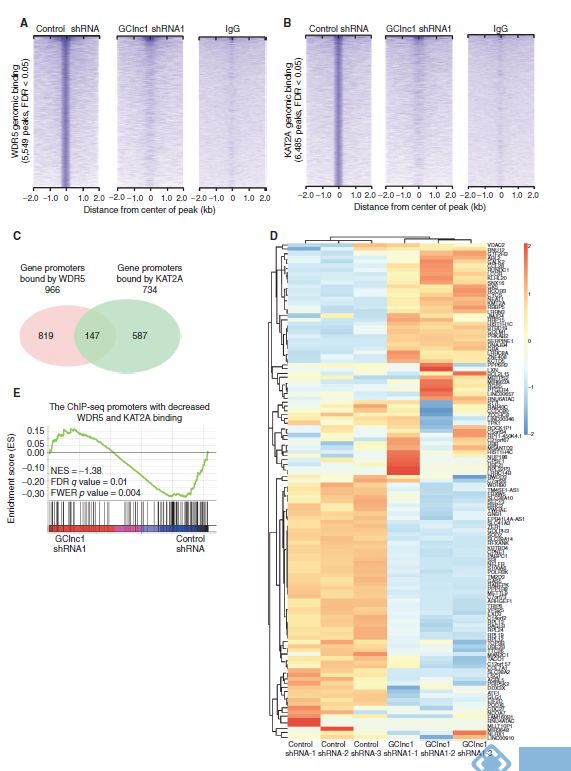
再接下来,作者利用ChIP-Seq方法去验证GClnc1是否可以调控蛋白WDR5和KAT2A在全基因组的结合位点。得到的结果是GClnc1敲低后会使WDR5和KAT2A在全基因组上的结合能力下降,并抑制相关基因的表达。因此敲低GClnc1会损害WDR5和KAT2A形成复合物,表明了GClnc1可以作为这种复合物的支架分子,从而调控组蛋白修饰、基因表达和生物学活性。
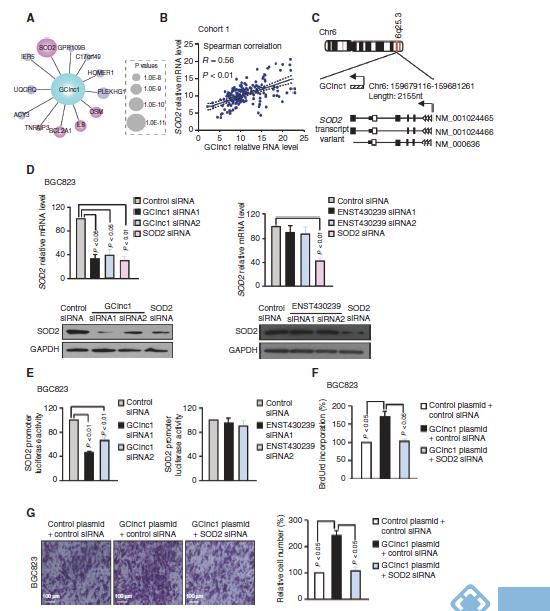
根据ChIP-Seq和RNA-Seq结果,作者发现SOD2是WDR5和KAT2A复合物的一个靶基因,并且发现GClnc1和SOD2具有高度正相关关系,并且利用CRISPR/Cas9去敲除SOD2,最终得到结论:SOD2确实在胃癌中受到GClnc1的调控。
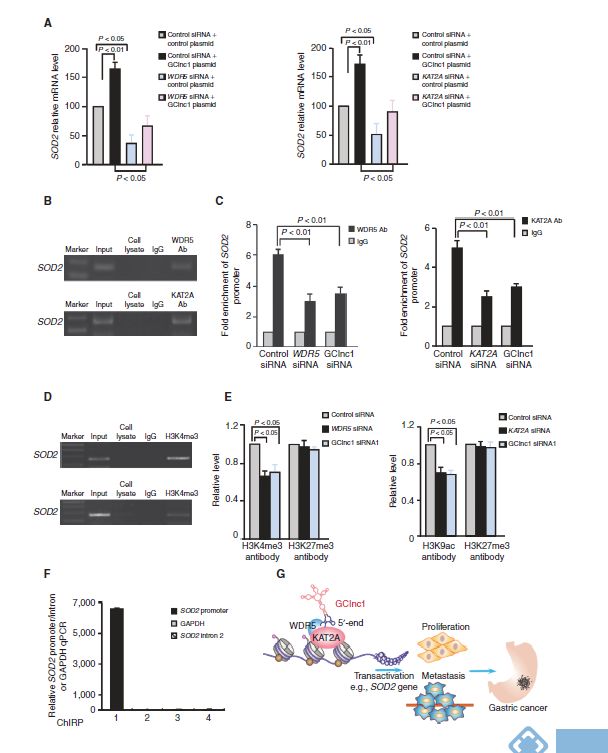
最终,作者想研究GClnc1是如何调控SOD2的,他猜测H3K4的甲基化和H3K9乙酰化可能调控SOD2的转录水平,RT-PCR和Westernblot实验也表明敲低WDR5或KAT2A可以减弱由GClnc1诱导的SOD2表达水平的上调。这些数据显示WDR5, KAT2A和GClnc1之间可以通过组蛋白修饰调控SOD2的转录活性,且ChIP实验也说明了WDR5和KAT2A可以直接结合在SOD2的启动子区域,敲低WDR5、KAT2A或GClnc1都会显著降低另外一种蛋白在SOD2上的结合能力,说明GClnc1可调控WDR5/KAT2A和SOD2启动子区域的结合能力。接下来的实验证明SOD2启动子区域存在H3K4me3和H3K9Ac,且GClnc1的表达水平的改变会让H3K4me3和H3K9Ac的丰度也发生变化。ChIRP分析显示GClnc1直接结合在SOD2的启动子区域。
结论:GClnc1可以做为一个支架把组蛋白修饰酶WDR5和KAT2A招募至SOD2的启动子处,从而激活该基因的转录,进而促进胃癌的发生和发展。
终于写到结尾了,大汗淋漓,一篇IF接近20的文章,做的工作之多可想而知,除了大样本的qPCR以外,还做了大量的功能性实验验证,这不仅需要实验设计者的高水平把控,还需要“装备精良”才可以,我们需要感激这些高水平的实验设计者,他们不仅花费了大量的人力物力去探究生命科学中的真谛,更重要的是为其他科研/临床工作者以及后来者指明了方向,也许我们做不到像此篇文章作者那样尽善尽美,但只要严谨踏实,用心做研究,终究你会爬到别人没有到过的山头,寻到属于自己独一无二的宝贝。
改一句古语:无赤心,不研究,研必有方,方为联川。
联川生物真心希望每一位科研/临床工作者付出必有回报,将生命科学之美散播人间。
Piccolo(运营部)丨文案
许洪荧丨编辑
图片及视频来自网络,侵删
怎么样,读了这篇文章是不是觉得自己get了高分文章的正确打开方式?
需要文章的小伙伴,欢迎回复文章题目至公众号,并留下您的邮箱,向小编免费索要哦~
“联川日”红包来袭~
关注“联川生物”公众号,1.26不见不散~