
文章导读:
近日,四川大学华西医院的周学东和袁泉研究组,联合中山大学第一附属医院的林水宾团队合作研究共同揭示了Mettl3介导m6A RNA甲基化调控骨髓间充质干细胞和骨质疏松症命运的新机制。该研究成果以Mettl3-mediated m6A RNA methylation regulates the fate of bone marrow mesenchymal stem cells and osteoporosis为题,于11月14日在《Nature communications》(IF:12.353)杂志在线发表。

研究思路
研究团队首先利用CRISPR-Cas9技术构建了MSCs有条件的敲除和敲入Mettl3的模型小鼠,然后微型CT和染色显示敲除后导致低骨量和高骨髓脂肪,并且MSCs中m6A整体甲基化水平也有所降低;同时,与执行了卵巢切除术的模型鼠相比,Mettl3过表达可预防雌激素不足引起的骨质疏松;接下来通过m6A MeRIP-seq和RNA-seq技术发现Mettl3缺失的MSCs存在PTH调控基因表达的全局下调,提示PTH/Pth1r信号轴可能是Mettl3介导的m6A甲基化对MSCs命运的影响通路。PTH间歇性注射实验也是印证了m6A通过调节PTH/Pth1r信号轴影响MSCs的成骨和脂肪分化的结论。另外,Pth1r的过表达可以在很大程度上逆转MSCs向脂肪细胞的倾斜分化,改善成骨,进一步证实了PTH/Pth1r信号通路是mettl3介导的m6A修饰控制MSCs谱系分配的新机制。
研究内容
1. MSCs 中Mettl3的敲除可导致低骨量、高骨髓脂肪
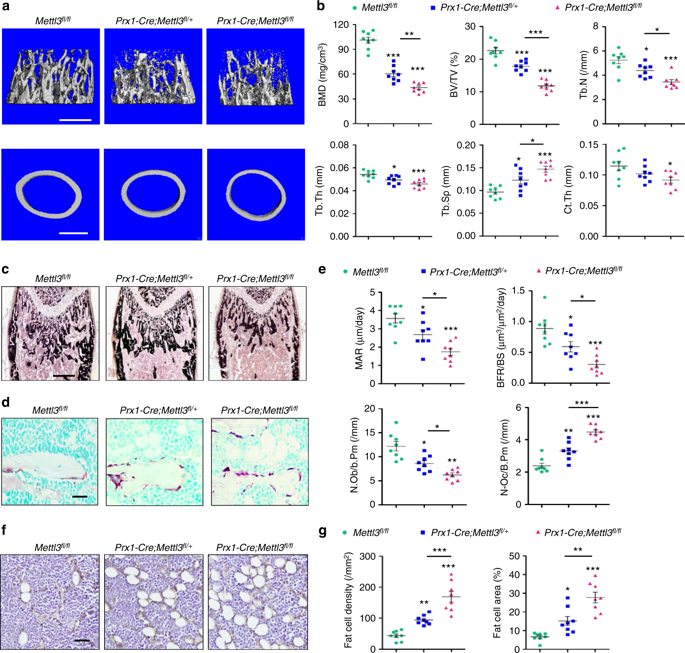
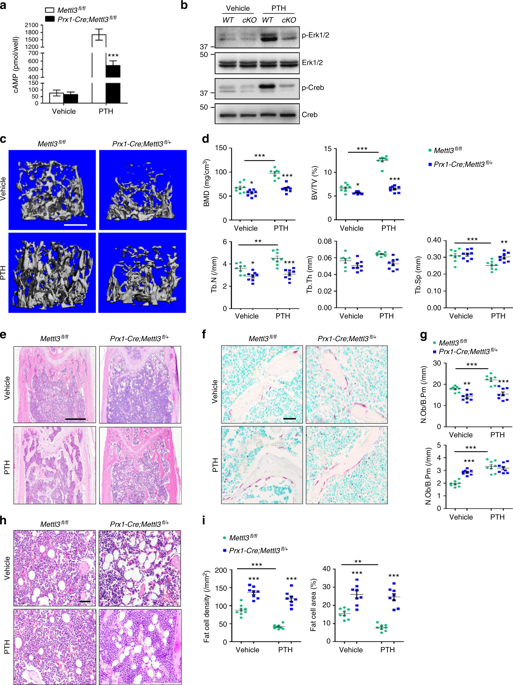
利用CRISPR-Cas9技术构建了MSCs有条件的敲除Mettl3的模型小鼠,股骨石蜡切片免疫染色和WB验证了Mettl3的敲除是的成功的。结果显示Mettl3敲除小鼠与对照组相比,骨质量损失且骨髓脂肪组织积聚显著,其骨骼特征与骨质疏松症的病理表型相似。同时LC-MS/MS检测发现MSCs中m6A甲基化整体水平下降。
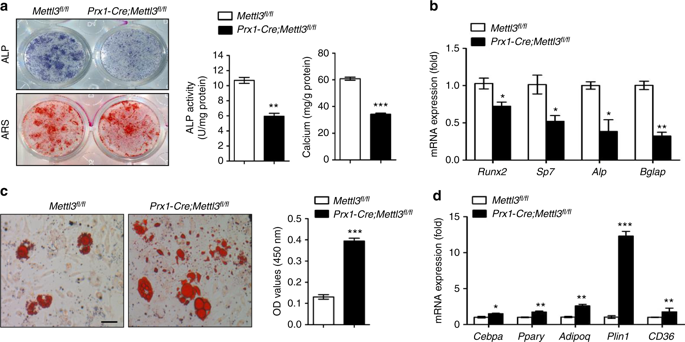
接下来,从Mettl3敲除的小鼠中分离出MSCs以验证其体外成骨和成脂潜能。碱性磷酸酶染色活性减弱,钙化减少,并且成骨标志物Runx2, Sp7, Alp和 Bglap 表达下调,表明缺失的MSCs成骨能力不强。相反,油红O染色强度的增加和显著的高表达是脂肪形成的潜在因素,包括Pparγ, Cebpα, Adipoq, Plin1和 CD36。
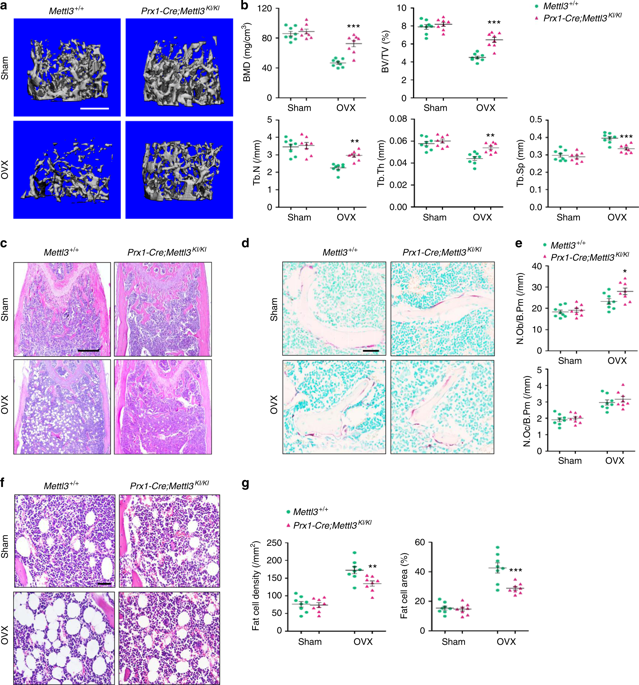
为了印证Mettl3过表达是否能够增强骨骼健康或预防骨骼疾病,在这里构建了MSCs中有条件的敲入Mettl3,使其在MSCs中过表达。通过卵巢切除术建立骨质疏松症实验模型,与对照相比Mettl3过表达增加了卵巢切除术后小鼠成骨细胞数量,但不影响破骨细胞活性。H&E染色和组织形态学分析显示,去卵巢的对照组小鼠骨髓脂肪细胞过度积累,而去卵巢的Mettl3敲入小鼠骨髓脂肪细胞的增加较小。
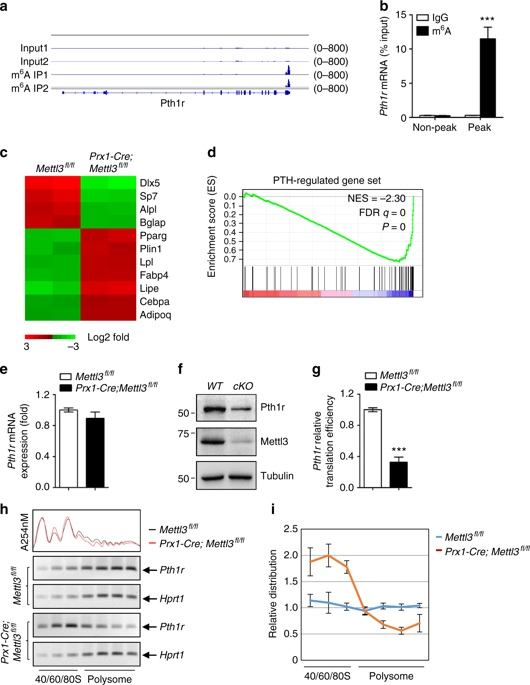
通过m6A MeRIP-seq技术对MSCs中m6A具体情况进行分析,结果显示m6A峰主要位于CDS和3’UTR区,并且主要位于终止密码子附近。还发现Pth1r是MSCs和成骨细胞前体中谱系分配的关键调控因子,在其翻译终止密码子附近具有高富集和特异性的m6A峰。RNA-seq发现Mettl3缺失的MSCs存在甲状旁腺激素(PTH)调控基因表达的全局下调,提示PTH/Pth1r信号轴可能是Mettl3介导的m6A甲基化对MSCs命运的影响通路。
Mettl3敲除的小鼠经PTH处理后骨重塑未见明显增强,证实敲除Mettl3可减弱PTH诱导的成骨作用。PTH除了在成骨过程中显著富集外,还能抑制脂肪细胞分化,促进骨形成。PTH间歇性注射显著降低了Mettl3敲除小鼠体内MAT的积累,但很难逆转Mettl3缺失小鼠中较高的骨髓脂肪含量;Pth1r过表达改善了m6A还原引起的油红O染色强度增加,显著提高ALP活性和钙结节形成。Pth1r的过表达可以在很大程度上逆转MSCs向脂肪细胞的倾斜分化,改善成骨,进一步证实了PTH/Pth1r信号通路是mettl3介导的m6A修饰控制MSCs谱系分配的新机制。
Mettl3介导的真核生物m6A RNA甲基化修饰对稳定体内稳态具有广泛的功能影响,而m6A水平的任何扰动都可能导致功能障碍或疾病。在这里研究证实了骨髓间充质干细胞中Mettl3的缺失破坏了小鼠的细胞命运,导致骨质疏松症病理表型如成骨潜能不全的骨量减少、成骨潜能增强的骨髓脂肪增多等,揭示了m6A对骨髓间充质干细胞的有效特异性调控。此外,Mettl3功能的增加可以预防雌激素不足引起的绝经后骨质疏松症,确立了Mettl3在确定骨髓MSC命运中不可或缺的作用,从而保证骨骼健康。早期骨髓间充质干细胞中m6A表观遗传修饰的减少抑制哺乳动物Pth1r的翻译,并在骨积累过程中阻断其对PTH的合成反应。这些功能缺陷使MSC微妙的分化平衡向脂肪谱系倾斜,导致严重的骨质流失和过度的MAT堆积。实验数据丰富了m6A调控干细胞分化的证据,揭示了调控不当的m6A修饰与骨病理障碍之间的功能联系,从而为骨质疏松症治疗新策略的开发提供了可能。
全文链接
https://www.nature.com/articles/s41467-018-06898-4
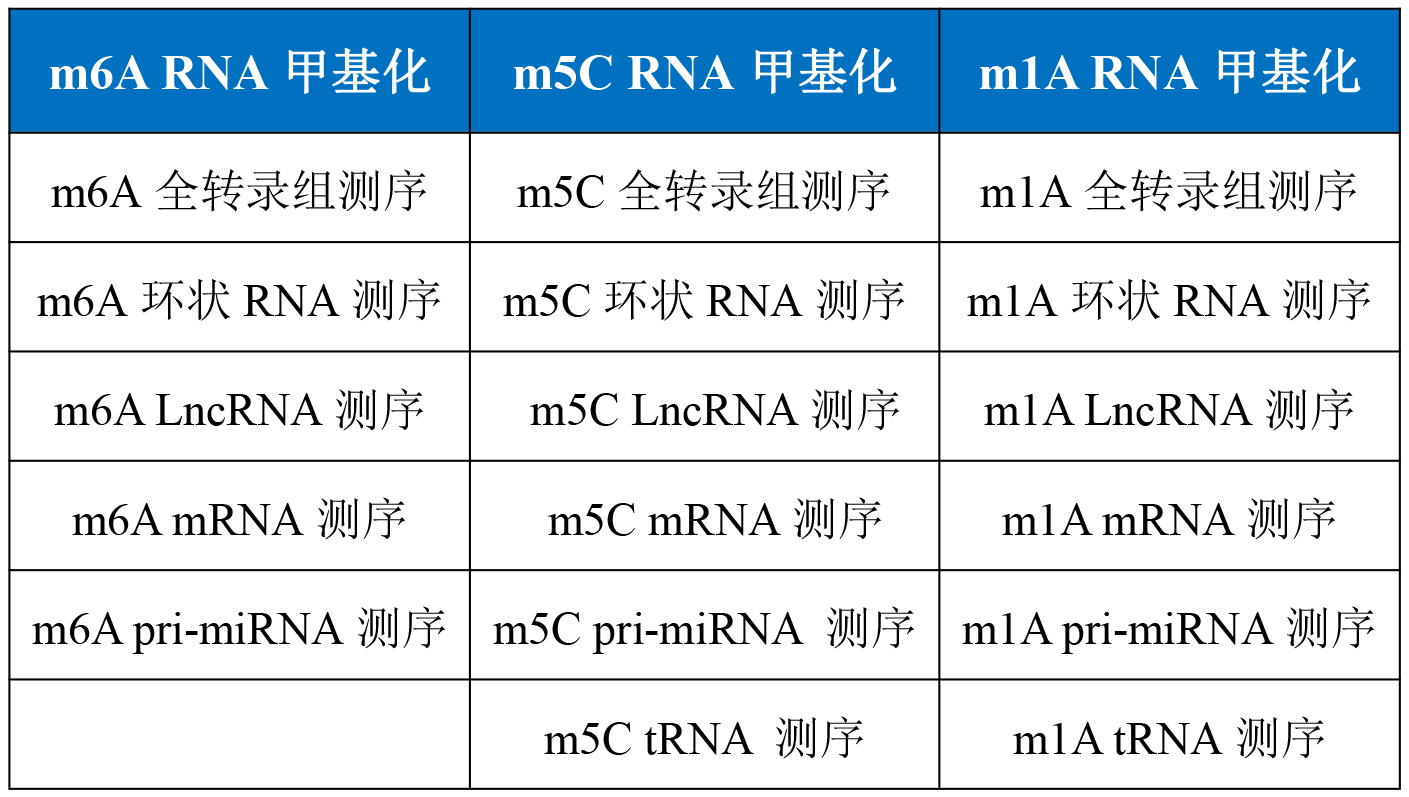
云序生物RNA甲基化产品列表:
云序相关产品推荐:
m6A RNA全转录组甲基化测序
m5C RNA全转录组甲基化测序
m1A RNA全转录组甲基化测序
超微量m6A甲基化测序
比色法检测整体甲基化水平
全转录组测序
往期回顾:
如何快速查找LncRNA序列
Nature|m6A RNA甲基化识别蛋白YTHDF1参与记忆的形成
10分以上m6A RNA甲基化测序文章----云序生物助力
不得了,大牛告诉你lncRNA甲基化如何研究
小白必看!RNA甲基化整体水平鉴定的方法汇总
20分文章中的RNA甲基化,热度与实力并存
云序生物最新m6A“RNA甲基化”研究汇总—非编码RNA篇
云序生物最新“RNA 甲基化”研究汇总-拟南芥篇
云序生物最新m6A“RNA甲基化”研究汇总—病毒篇
Plant Cell:拟南芥发现全新m6A RNA去甲基化修饰酶
云序客户12分顶级文章,教你如何巧用RIP测序玩转分子机制!
2018年Nature杂志重磅级突破性研究成果--m5C RNA甲基化 云序生物
Nature突破性研究—RNA甲基化新修饰m1A 云序生物
Hepatology:m6A RNA甲基化酶METTL3促肝癌发展新玄机
云序生物独家m5C RNA甲基化测序
Nature文章揭示RNA甲基化多重功能
填补表观遗传修饰空白:RNA甲基化调控基因出核新机制
上海云序生物科技有限公司
Shanghai Cloud-seq Biotech Co., Ltd.
地址:上海市松江区莘砖公路518号20号楼3楼
电话:021-64878766
传真:021-64878766
网址:www.cloud-seq.com.cn
邮箱:market@cloud-seq.com.cn
