先前我们简单回顾了一下CRISPR/Cas系统的发展历史。那么基因编辑究竟在哪些方面能够发挥它的神奇能力呢?
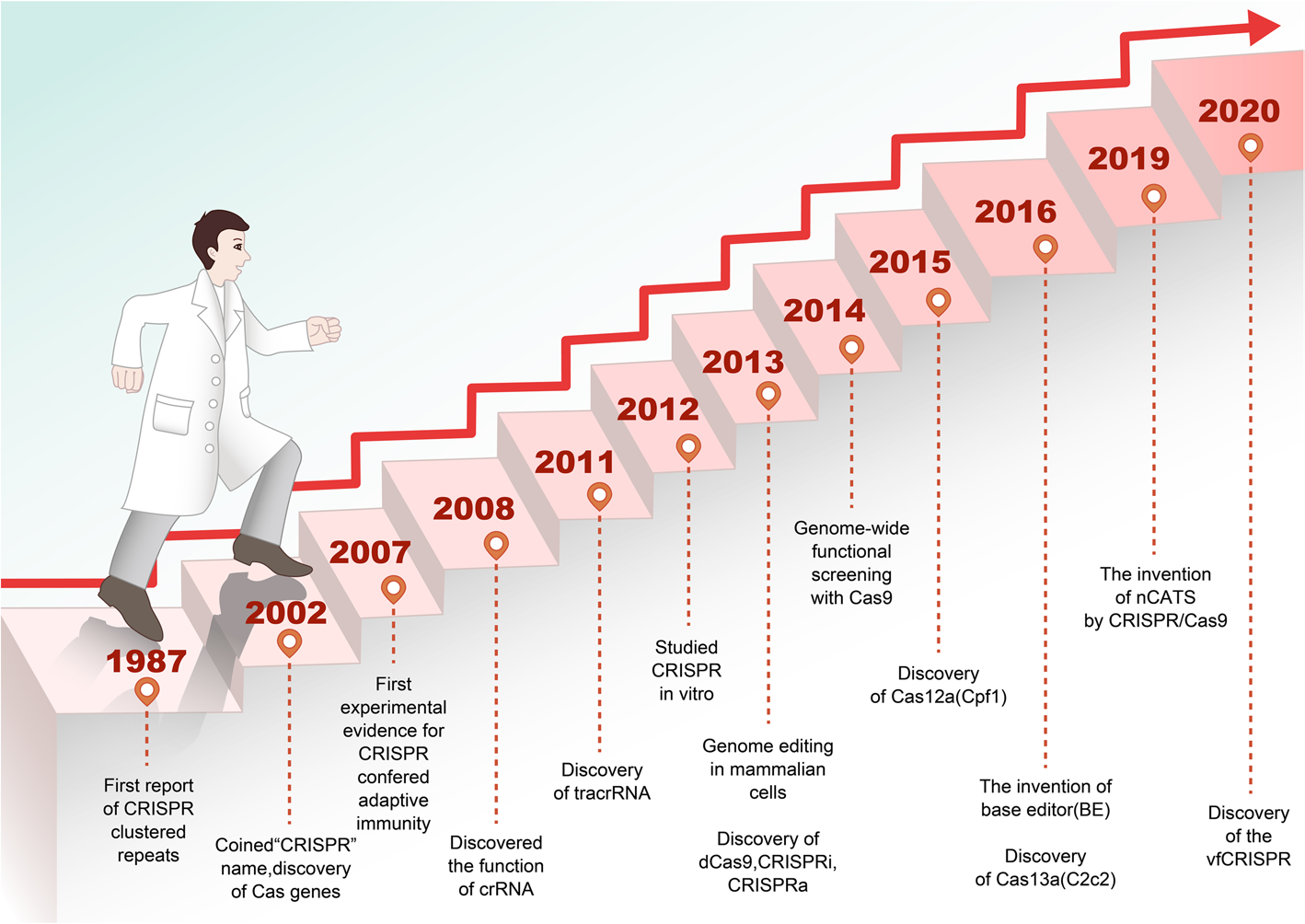
基于CRISPR/cas9的基因编辑工具的发展历史
(图片来自“Application of the CRISPR/Cas9-based gene editing technique in basic research, diagnosis, and therapy of cancer”.)
无论是重大疾病的治疗,还是农作物超级品种的培育,都是关乎人类社会未来发展的重要命题。
一、CRISPR/Cas系统在癌症研究中的应用
癌症的起始和进展涉及一系列基因的突变和异常表达,包括致癌基因、肿瘤抑制基因、化疗耐药基因、代谢相关基因和癌症干细胞相关基因。癌症治疗的最终目标是通过特异性纠正突变和恢复失调基因的表达来抑制肿瘤的生长和进展。在过去的20年里,高通量测序技术发现了大量与癌症起始和进展相关的基因。基于这些进展,基因编辑技术有望通过调节基因表达和纠正基因突变来治疗癌症,这可能会导致精准肿瘤领域的进一步突破。
早期诊断
CRISPR/Cas9在癌症诊断中的应用
——通过基因诊断来识别敏感基因是预防癌症的关键。

研究团队利用CRISPR/Cas9敲除致癌突变EGFR等位基因,发现肺癌细胞系H1975、A549和H1650的生长和增殖被抑制,植入H1975或A549细胞的异种移植小鼠肿瘤尺寸减小。
靶向治疗
研究表明,CRISPR/Cas9基因编辑系统是识别癌基因和评估癌基因靶向治疗潜力的有效工具。

激活抑制基因
修复失活的肿瘤抑制基因——识别并激活抑癌基因,抑制癌变通道

该研究团队使用CRISPR/dCas9与反式激活因子VP64-p65-Rta(VPR)联合使用,激活低水平PTEN表达的癌细胞中PTEN的表达。结果显示,dCas9-VPR系统提高了黑色素瘤和TNBC细胞系中PTEN的表达水平,而PTEN的激活明显抑制了下游的致癌通路。
调节癌细胞耐药性
解决癌细胞对化疗药物的耐药性问题
——识别化疗耐药相关基因并调节其表达水平或功能

CRISPR/Cas9在NSCLC细胞系中敲除AURKB,也恢复了肿瘤抑制基因TP53的表达以及对顺铂和紫杉醇(两种化疗药物)的敏感性。
了解代谢机制
关于代谢基因——肿瘤细胞依赖于足够的能量供应来支持增殖、迁移和侵袭,了解能量代谢机制可能为我们在癌症治疗中靶向能量产生途径提供新的思路。

采用CRISPR/Cas9系统敲除HEp-2细胞中的HIF-1α和GLUT−1基因,导致增殖、迁移和侵袭减少。Tey发现,HIF-1α和GLUT-1基因敲除可显著降低HEp-2细胞的葡萄糖摄取和乳酸。
肿瘤干细胞相关基因
肿瘤干细胞(CSC)是肿瘤中自我更新的细胞,可以产生异质性肿瘤细胞,在癌症的发生、进展、复发和治疗耐药性中发挥关键作用。由于CSC可能来源于癌基因的重编程和癌细胞的动态特性,因此推测CSC相关基因的鉴定将产生新的癌症治疗靶点。目前,CRISPR技术在肿瘤干细胞中的应用为临床肿瘤治疗提供了新的方向。
阐明癌症的起因与发展
利用CRISPR/Cas9库筛选癌细胞中的功能基因——癌细胞基因组携带多种遗传变异,这些变异由先天性和后天突变积累,并由连续的克隆扩展触发。识别驱动肿瘤进化的基因可以阐明癌症的起始和发展。使用CRISPR进行功能基因组筛选可以揭示药物治疗后的表型变化,从而确定癌症治疗的新靶点。
癌症建模
CRISPR/Cas9在癌症建模中的应用
——CRISPR/Cas9能够在体内构建具有多个基因突变的肿瘤模型,从而更好地模拟复杂的人类疾病,这种新兴的建模方法可以对体内外癌症基因进行更有效的研究。
浙江大学平渊研究员和华东师范大学程义云教授开发了一种基于CRISPR-Cas9的基因组编辑纳米药物,并将其用于靶向APC和KRAS突变以治疗结直肠癌。

2021年12月3日,广西医科大学赵永祥团队发表题为“Generation of in situ CRISPR-mediated primary and metastatic cancer from monkey liver”的研究论文,该研究产生了一种原位基因编辑方法,以诱导Pten和 p53基因的有效功能丧失突变,用于在成年食蟹猴中使用CRISPR/Cas9 快速建模原发性和转移性肝肿瘤。这有望成为一种强大而可行的工具,用于编辑疾病基因在成人NHP中建立相应的人类疾病模型,大大加快新药的发现并节省经济成本。
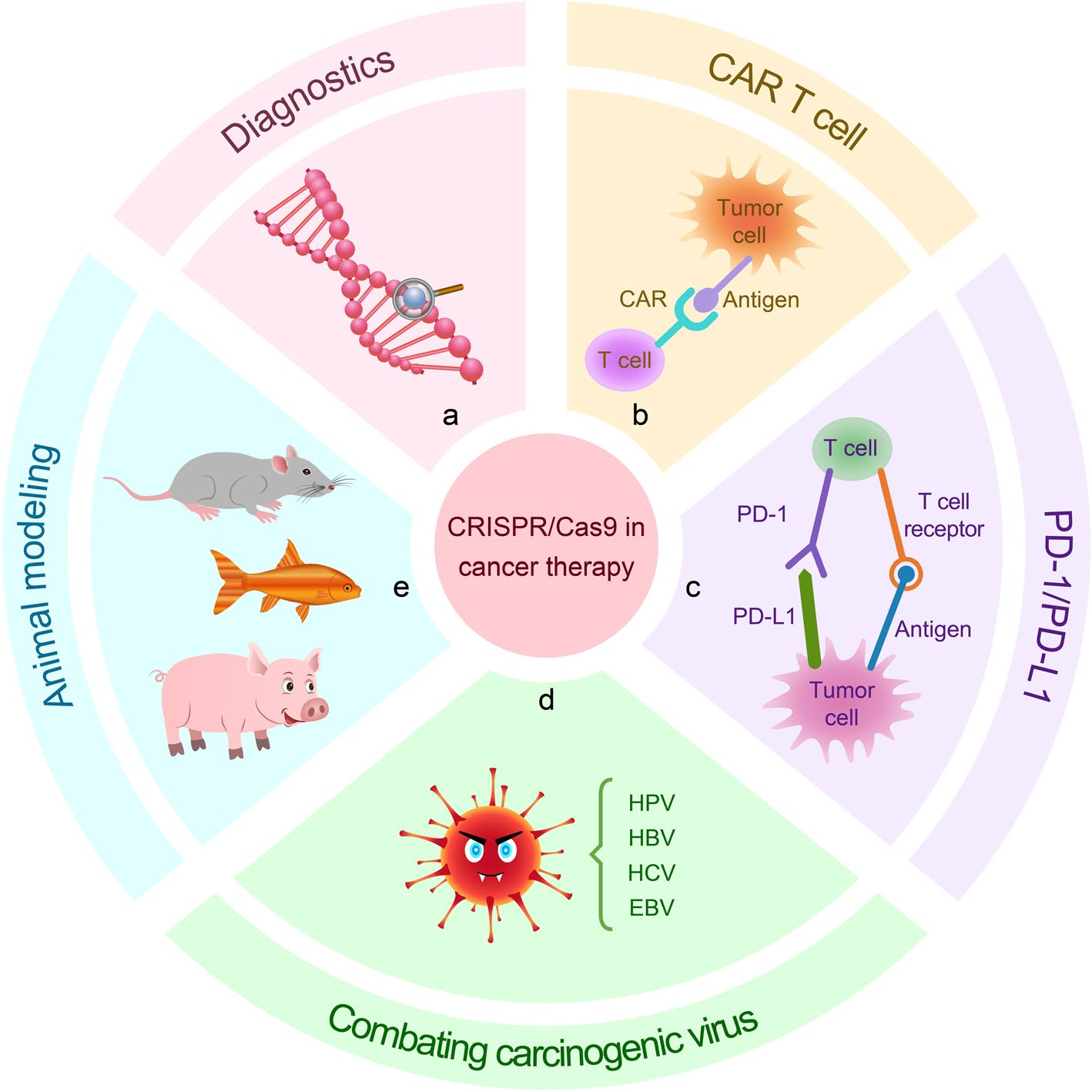
CRISPR/Cas9基因编辑工具在癌症诊断和治疗中的应用
(图片来自“Application of the CRISPR/Cas9-based gene editing technique in basic research, diagnosis, and therapy of cancer”.)
二、CRISPR/Cas系统在植物技术研究中的应用
通过基因组工程对植物的遗传控制使功能基因组学的生长和作物物种的遗传改良成为可能。目前,该系统已在世界各地的许多实验室中使用,主要用于简单地敲除基因,以产生所需的突变体或具有改良农业性状的新种质材料。它对植物科学产生了革命性的影响。与其他育种技术相结合,CRISPR/Cas9将有助于培育超级品种,以满足未来几十年人口增长的需求。
粮食作物:小麦
发表刊物:《Plant Biotechnology Journal》
标题:CRISPR/Cas9-mediated genome editing for wheat grain quality improvement
研究团队:山东省农业科学院作物研究所李根英研究员领衔的小麦分子育种创新团队
研究选取了与小麦加工品质密切相关的四个基因(籽粒硬度基因pinb、淀粉品质基因waxy、面粉色泽基因psy和面团褐变基因ppo),利用农杆菌介导的CRISPR/Cas9系统对其进行精准打靶,经过多代纯合和鉴定,获得不含外源转基因成分的基因编辑新种质,为小麦品质育种提供了新的基因资源。

粮食作物:水稻
发表刊物:《Plant Biotechnology Journal》
标题:Production of aromatic three-line hybrid rice using novel alleles of BADH2
研究团队:中国水稻研究所胡培松院士团队
该研究通过CRISPR/Cas9基因编辑技术创制新型BADH2等位基因系,对三系杂交稻的香味改良进行了大胆实践,为三系杂交稻香味性状改良提供了新思路。

粮食作物:高粱
发表刊物:《Plant Biotechnology Journal》
标题:CRISPR/Cas9-mediated genome editing for wheat grain quality improvement
研究团队:来自加州伯克利大学的Peggy G. Lemaux教授团队
传统的高粱转化方法在验证高粱功能方面存在基因型依赖和选择、再生和世代推进时间长的障碍。本研究通过改良MAT技术,使得高粱转化效率更高,转化植株的时间缩短,为验证高粱中许多未表征的基因功能提供了直接的手段。该研究找到的是一种对难以进行遗传转化作物的有效转化方法,并提高了转化效率缩短了转化时间,加速了对广泛生长、多用途作物的多种基因型的研究。

三、结 语
CRISPR基因编辑技术自问世以来,就以无可比拟的优势,深刻改变了基因编辑领域乃至整个生命科学的研究模式。如今,CRISPR技术已被应用于精确基因组编辑和转录调控等一系列科学研究,这使得科学家能够“随意”操纵基因序列。
不仅如此,基于CRISPR技术的基因疗法已经开始应用于临床治疗,特别是一些由基因突变引起的疾病,例如遗传病和癌症。
然而,一些研究却表明,CRISPR技术存在重大的潜在风险,包括脱靶效应、染色体改变和潜在免疫原性等。脱靶效应是CRISPR/Cas9基因治疗的明显缺陷,无关的细胞吸收了CRISPR/Cas9有“大 | 麻烦”,如果将通过CRISPR/Cas9基因编辑的细胞用于治疗,将会有潜在致癌性风险,要想解决潜在致癌性这个问题,或许要先解决基因编辑技术面临的核心难题—脱靶效应。使用CRISPR-Cas9时,要重点监测癌症相关基因突变,特别是p53基因和KRAS基因。
机遇与挑战向来是共存的,虽然有潜在风险,但CRISPR基因编辑仍是一项蓬勃发展的革命性技术。
参考文献
1. Huimin Zhang,,et al(2021). Application of the CRISPR/Cas9-based gene editing technique in basic research, diagnosis, and therapy of cancer. Mol Cancer (2021) 20:126. https://doi.org/10.1186/s12943-021-01431-6
2. Li, Y., Li, W., & Li, J. (2021). The CRISPR/Cas9 Revolution continues: From base editing to prime editing in plant science. Journal of Genetics and Genomics, 48(8), 661–670. https://doi.org/10.1016/j.jgg.2021.05.001
