近期还有测序免费送活动,详情点击庆云序MeRIP-seq文章超65篇,MeRIP-seq满五送 一 (cloud-seq.com.cn)
一、大鼠缺氧性肺动脉高压模型中lncRNAs的m7G修饰谱

发表日期:2022年1月7日
研究方法:m7G-MeRIP-seq、RNA-seq、MeRIP-PCR
样品类型:大鼠缺氧性肺动脉高压肺组织(3) vs 大鼠常氧肺组织(3)
文章链接:N7-methylguanosine modification of lncRNAs in a rat model of hypoxic pulmonary hypertension: a comprehensive analysis
技术路线
1、缺氧性肺动脉高压和对照组中lncRNA m7G甲基化的整体修饰特征
首先对缺氧性肺动脉高压(HPH)和对照(常氧,N)大鼠的肺组织进行m7G-MeRIP-seq和lncRNA-seq,测序结果显示,两组间共有255个m7G甲基化峰,仅占两组所有峰的5.0%,百分比较低,表明两组间m7G模式存在差异。分析各lncRNA中m7G峰个数的分布,两组间无显著差异。进一步分析m7G甲基化的lncRNA外显子数量,发现在HPH和对照组中,超过30%的总lncRNA包含两个外显子。同样,m7G和非m7G lncRNA主要由两个外显子编码,说明HPH组和对照组的两个外显子对lncRNA中m7G甲基化的贡献最大。
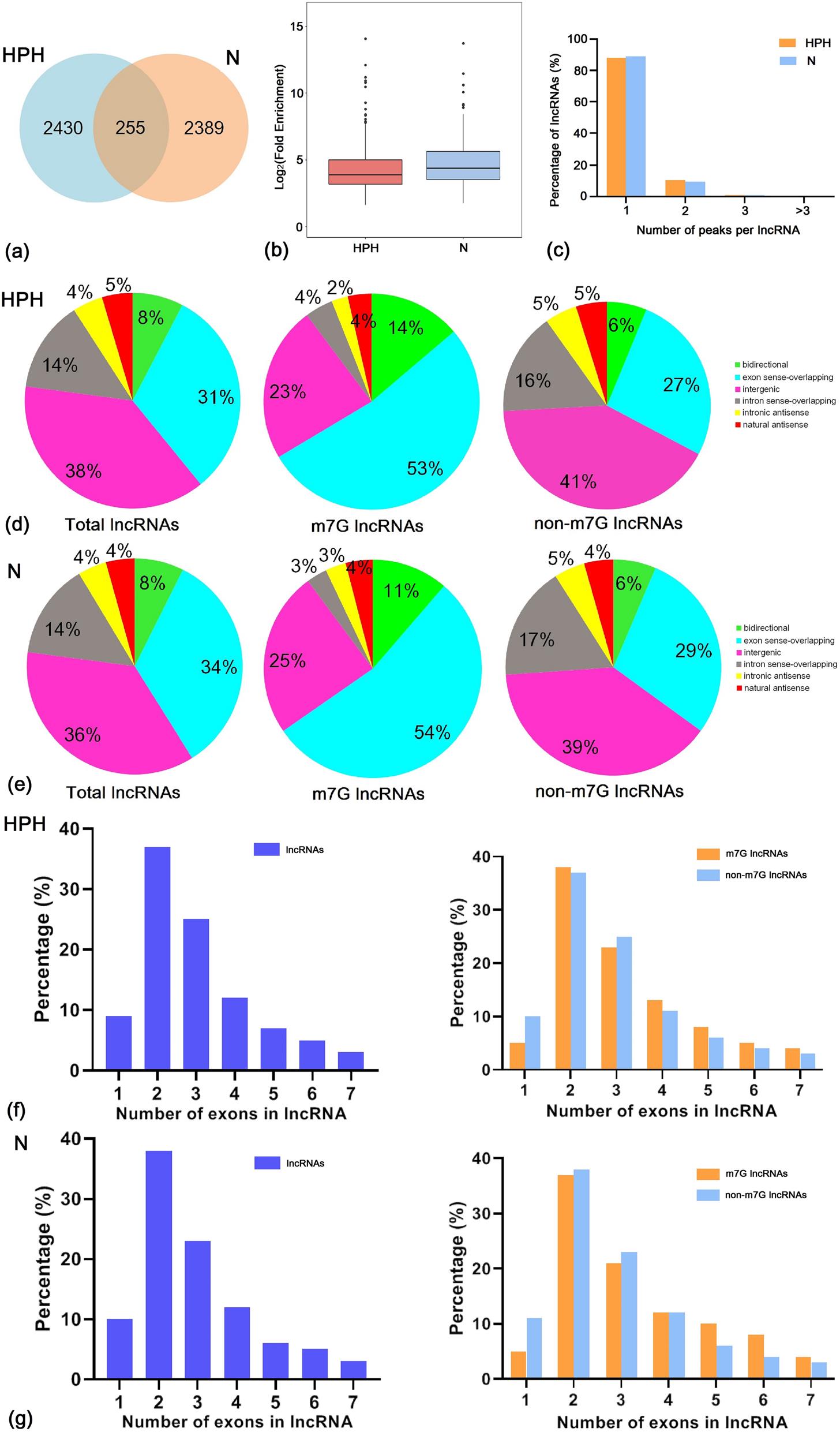
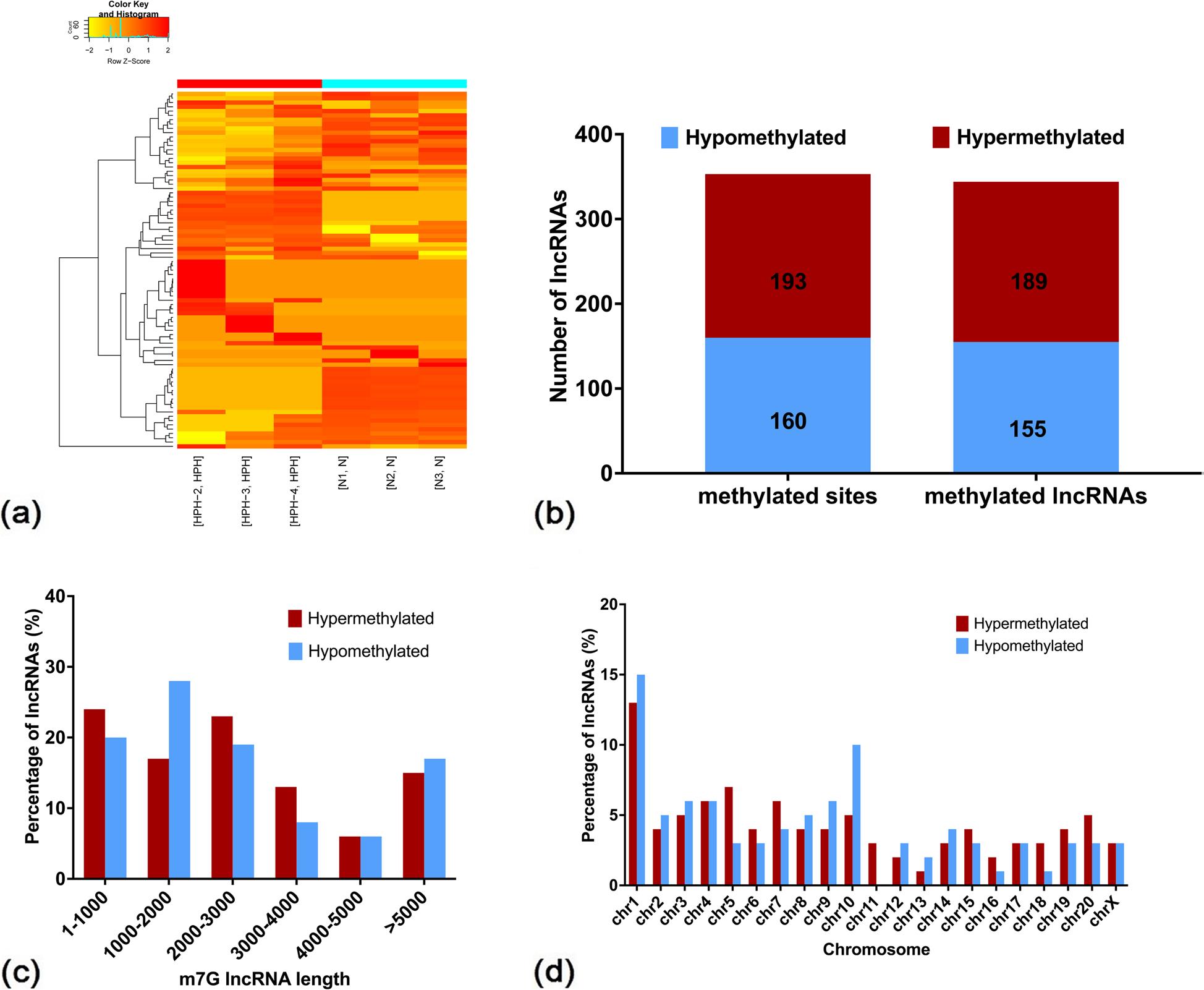
2、两组间差异甲基化lncRNA的长度和分布
如m7G lncRNA表达的热图所示,344个lncRNA中鉴定出353个差异甲基化的m7G位点。其中55%显著高甲基化,45%显著低甲基化。对差异甲基化lncRNA的长度分析显示,高甲基化和低甲基化类型之间存在差异。接下来还分析了差异甲基化lncRNA在染色体上的分布,其中低甲基化的m7G lncRNA主要位于1、5和4号染色体,低甲基化的m7G lncRNA主要位于1、10和3号染色体。
为了阐明差异甲基化lncRNA在缺氧性肺动脉高压发生发展中的作用,作者还对位于差异甲基化lncRNA临近基因进行了GO和KEGG通路分析。GO结果显示,高甲基化lncRNAs临近基因主要参与补体激活、胞内细胞成分等。位于低甲基化lncRNAs临近基因主要与蛋白糖基化、肌细胞分化、免疫球蛋白分泌等相关。此外,KEGG通路分析显示,这些差异甲基化基因主要与金黄色葡萄球菌感染、cGMPPKG信号通路等通路相关。综上,m7G修饰的lncRNA可能通过以上GO功能和信号通路影响HPH的发生发展。
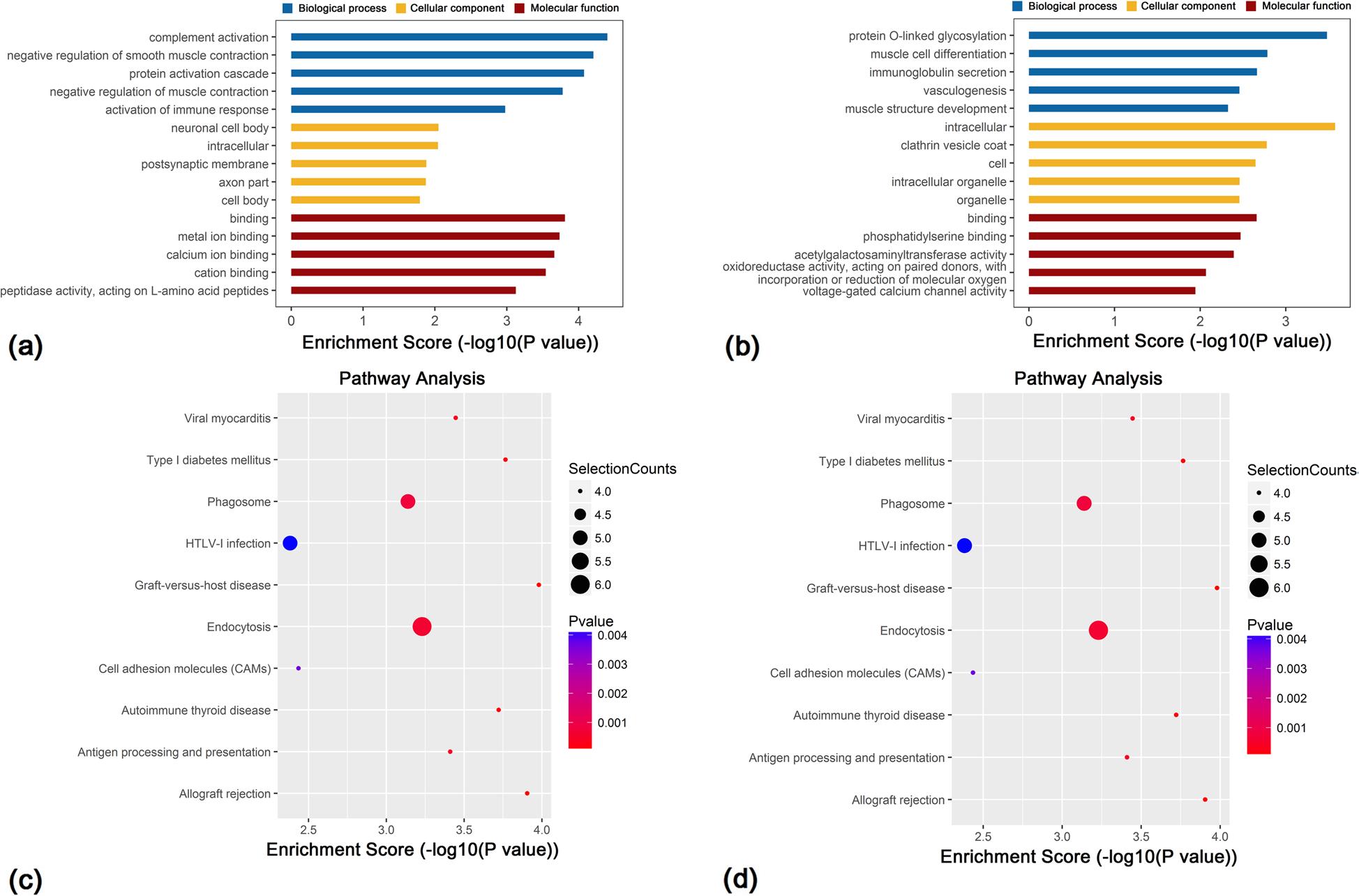
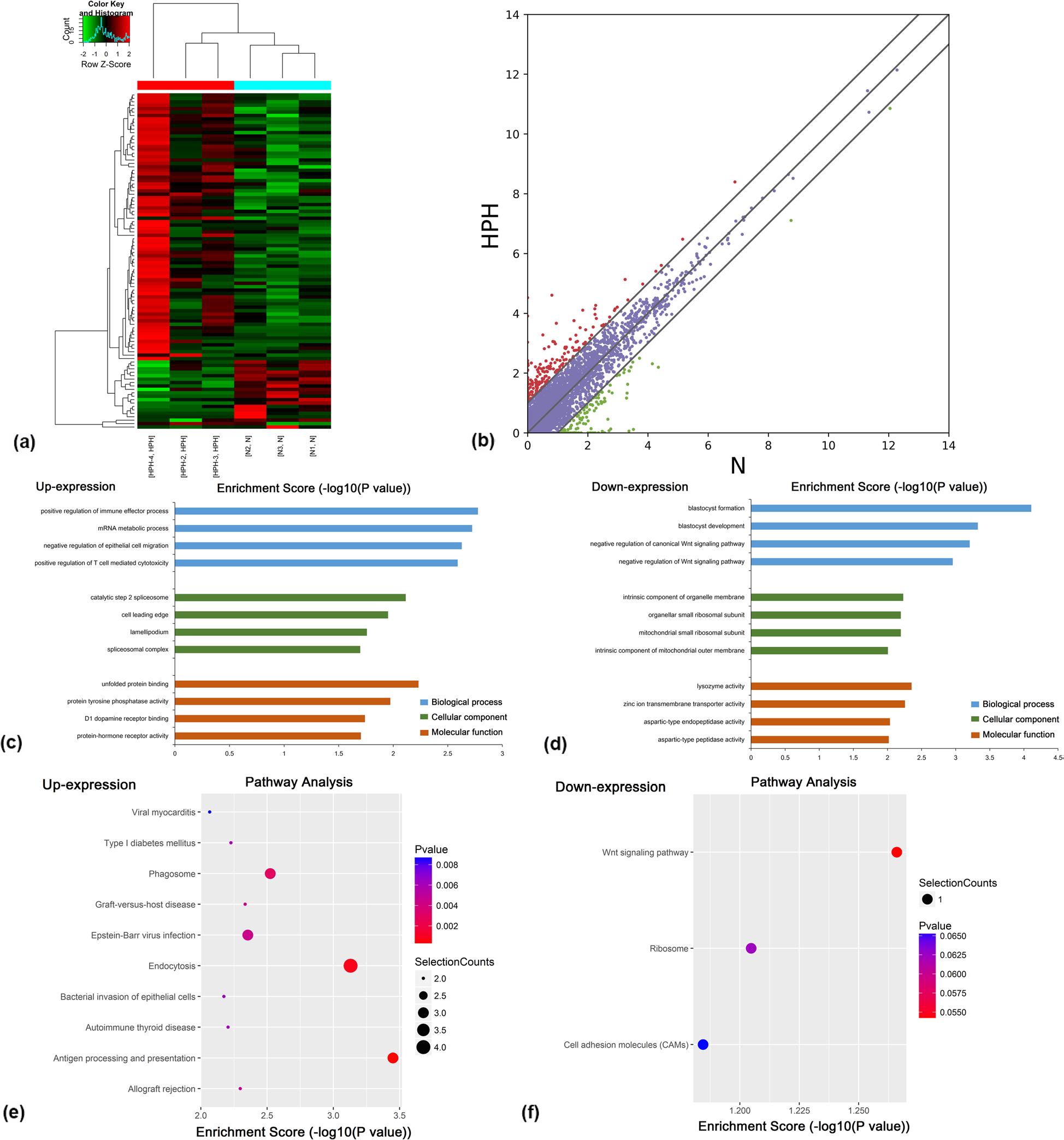
4、RNA-seq分析HPH中的lncRNA表达谱
通过lncRNA-seq分析了两组lncRNA的表达情况。共有111个lncRNA在HPH组中显著差异表达,其中90个上调,21个下调。同样预测了这些差异表达lncRNA临近基因的功能。GO分析显示,差异表达基因主要与免疫效应过程、囊胚形成、、和细胞器膜固有成分显著相关。此外,KEGG通路分析显示,主要参与抗原加工呈递、内吞和吞噬作用以及Wnt信号通路。总之,这些结果表明,HPH中差异表达的lncRNA可能与HPH发病机制相关。
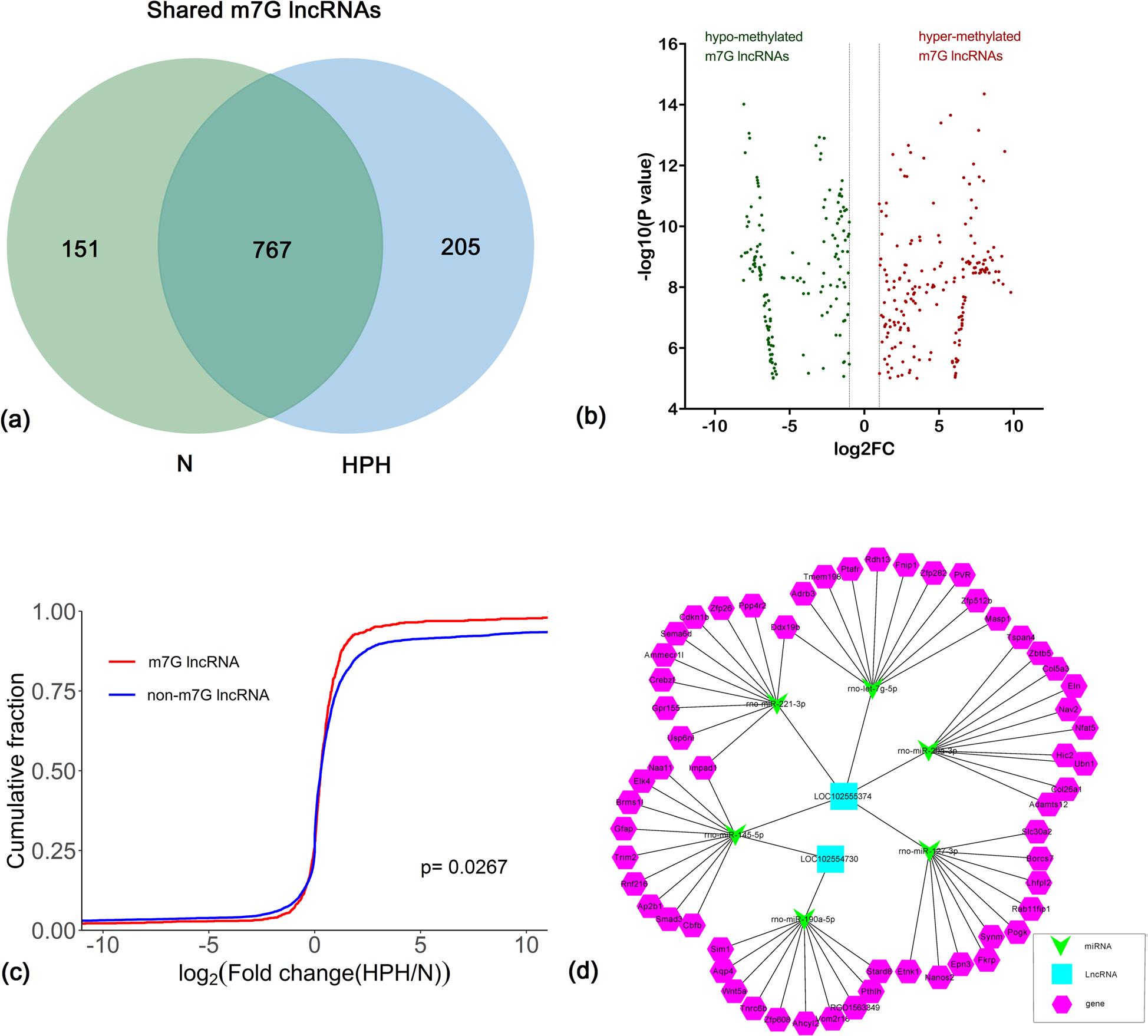
为了探究lncRNA甲基化与表达之间的关系,对m7G MeRIP-seq和lncRNA-seq数据进行了联合分析。重点研究了两组间均有的767个m7G lncRNAs的表达,以分析缺氧对m7G甲基化修饰的影响。与对照组相比,HPH中发现了189个高甲基化和155个低甲基化的m7G lncRNA,且m7G-lncRNA所占比例大于非m7G-lncRNA。这些结果表明,在缺氧条件下,m7G修饰显著上调了lncRNA的表达。联合分析显示,只有两个表达上调的lncRNA被高甲基化,LOC102554730(XR_591973)和LOC102555374(XR_592398)。通过构建ceRNA网络,发现预测的这六个miRNA均与肺动脉高压相关。
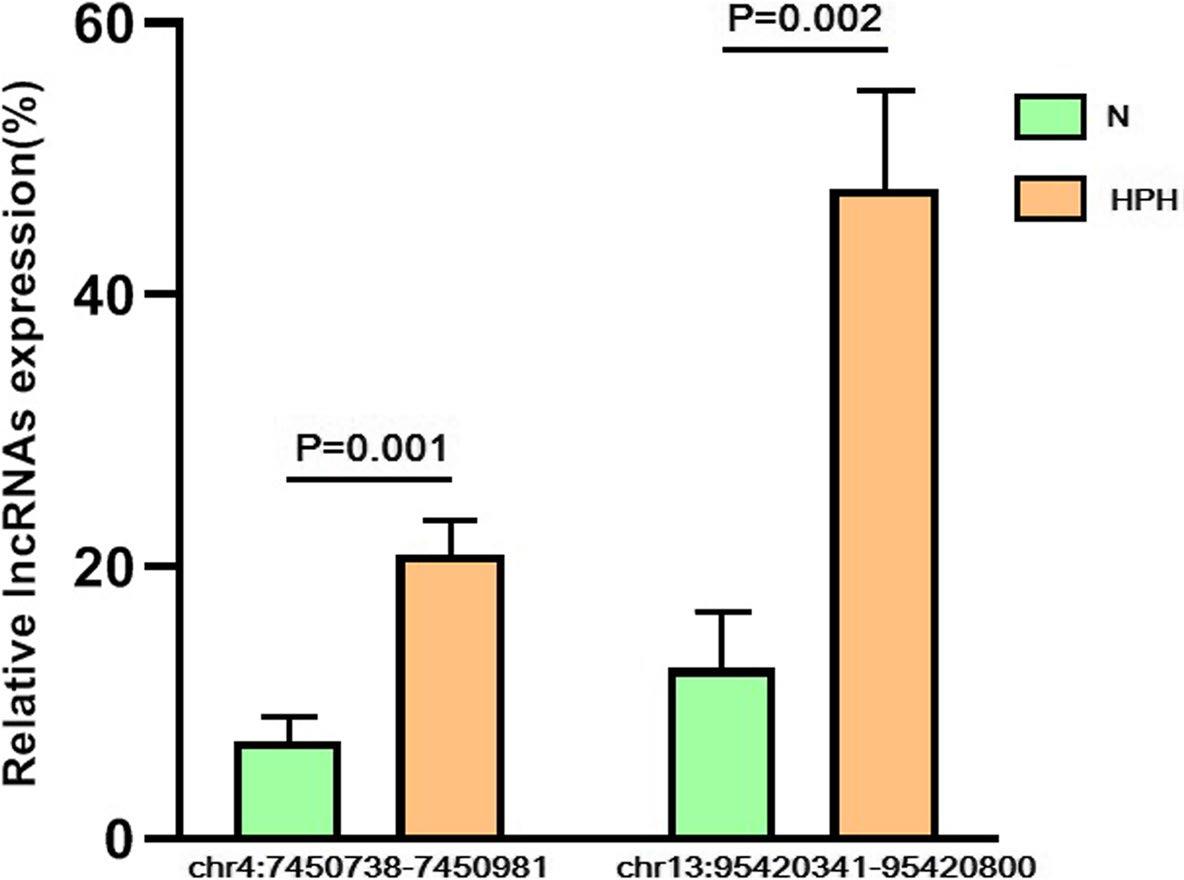
为了进一步证实这一结果,作者验证了两种差异表达的m7G lncRNAs在缺氧(1% O2)和常氧(21% O2) 肺动脉平滑肌细胞中的表达。通过MeRIP-PCR技术检测lncXR_591973和lncXR_592398是否经m7G修饰,结果显示m7G lncXR_591973和m7G lncXR_592398水平显著升高,证明了m7G-MeRIP-seq分析的可靠性。

发表日期:2022年2月8日
研究方法:m7G-MeRIP-seq、m5C-MeRIP-seq、m6A-MeRIP-seq、m1A-MeRIP-seq、RNA-Seq
样品类型:斑马鱼缺氧脑组织 vs 斑马鱼常氧脑组织
文章链接:Mapping the m1A, m5C, m6A and m7G methylation atlas in zebrafish brain under hypoxic conditions by MeRIP-seq
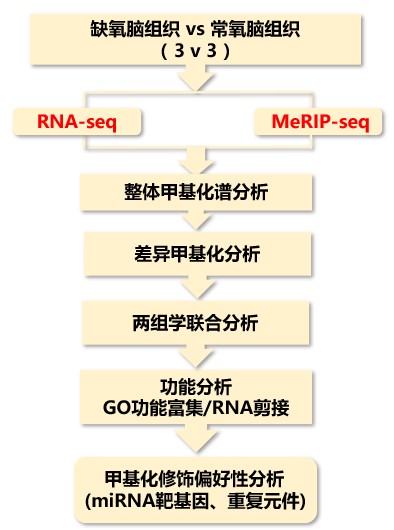
研究内容
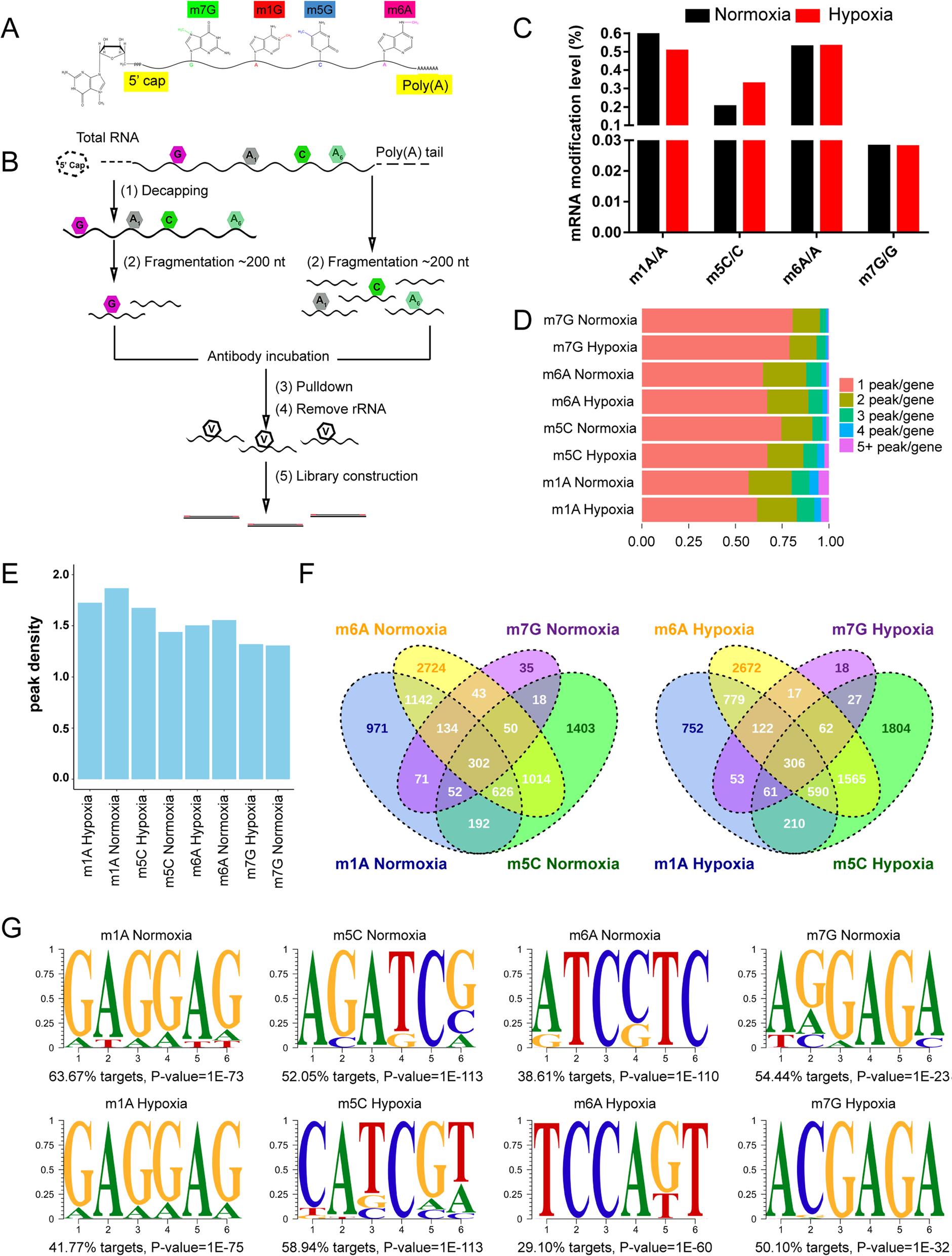
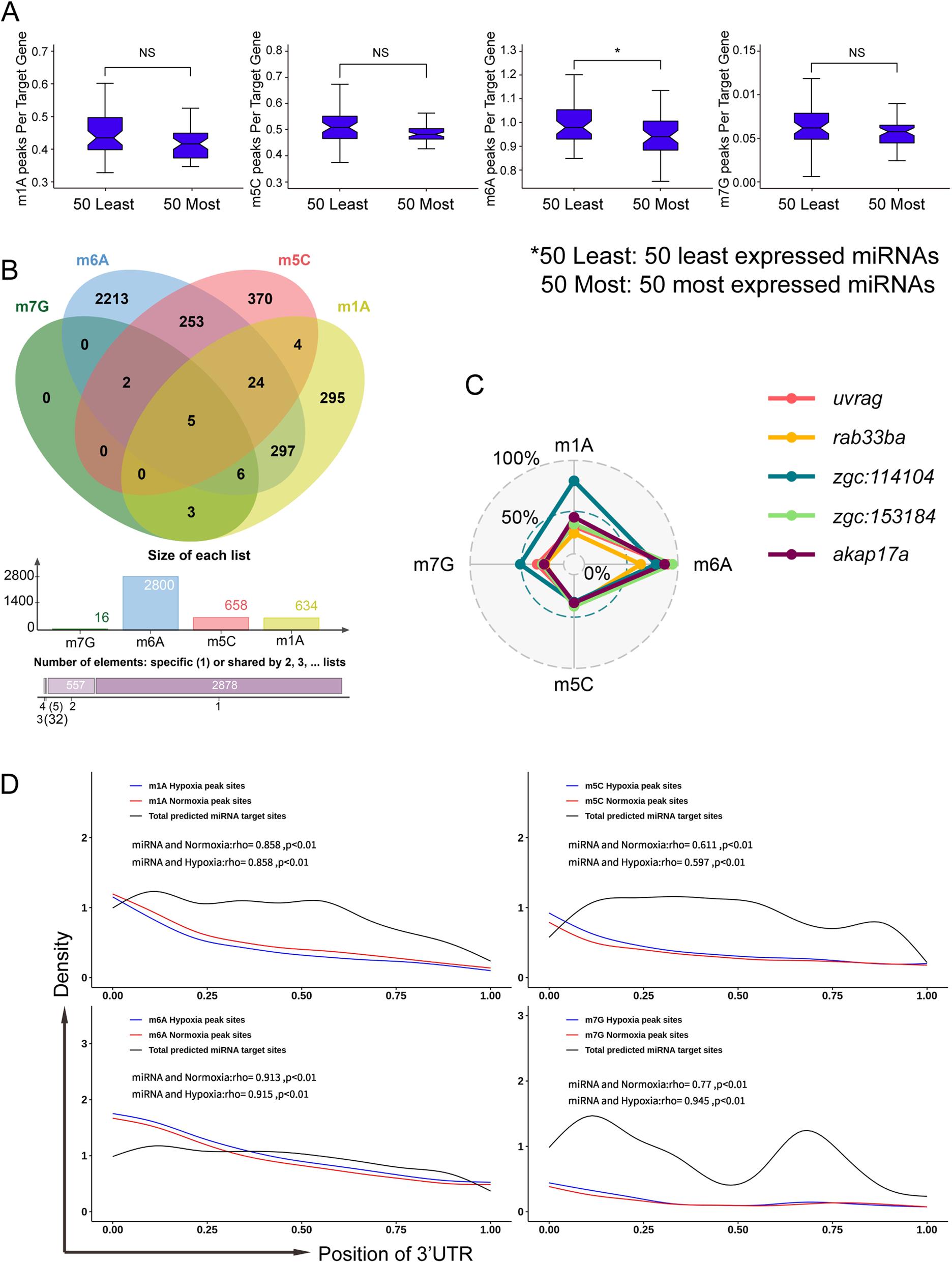
1、缺氧条件下斑马鱼脑中m1A、m5C、m6A和m7G的甲基化丰度为了研究斑马鱼大脑中的mRNA甲基化图谱以及揭示缺氧诱导后大脑mRNA甲基化修饰的改变,分别采取经常氧或低氧处理的斑马鱼大脑进行RNA-Seq、m7G-MeRIP-seq、m5C-MeRIP-seq、m6A-MeRIP-seq、m1A-MeRIP-seq等检测。测序结果显示,m1A、m5C、m6A和m7G四种RNA甲基化修饰均广泛分布于斑马鱼脑的mRNA中,其中m1A和m6A修饰水平相对较高。在缺氧条件下,m1A降低、m5C升高;而m6A和m7G变化不大。motif分析发现m1A和m7G mRNA峰都倾向于具有富含GA的基序,但在缺氧和常氧条件下,m5C和m6A motif存在一些差异。
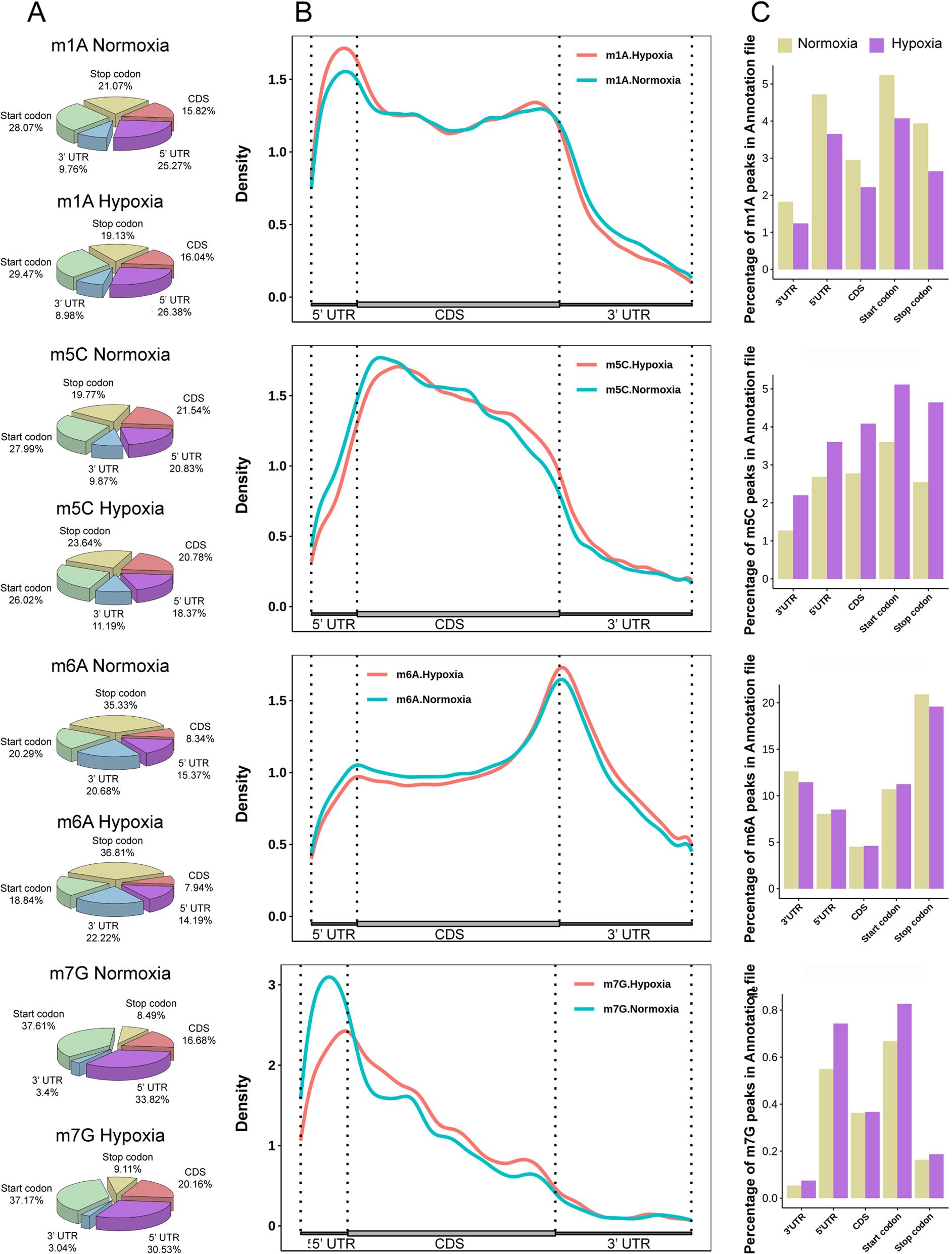
为了更好地了解m1A、m6A、m5C和m7G位点在斑马鱼脑组织中的分布,分析了其在基因组上的分布特征。发现m1A和m7G倾向于富集在5’UTR和起始密码子区域,而m5C富集在CDS区域,m6A富集在终止密码子附近。此外, m1A丰度在缺氧的CDS区下调,而m5C丰度在缺氧的CDS区上调。m6A丰度无差异,但5’UTR和起始密码子区域中m7G丰度下调。以上结果表明,在缺氧条件下,斑马鱼脑组织的四种甲基化修饰表现出显著差异。
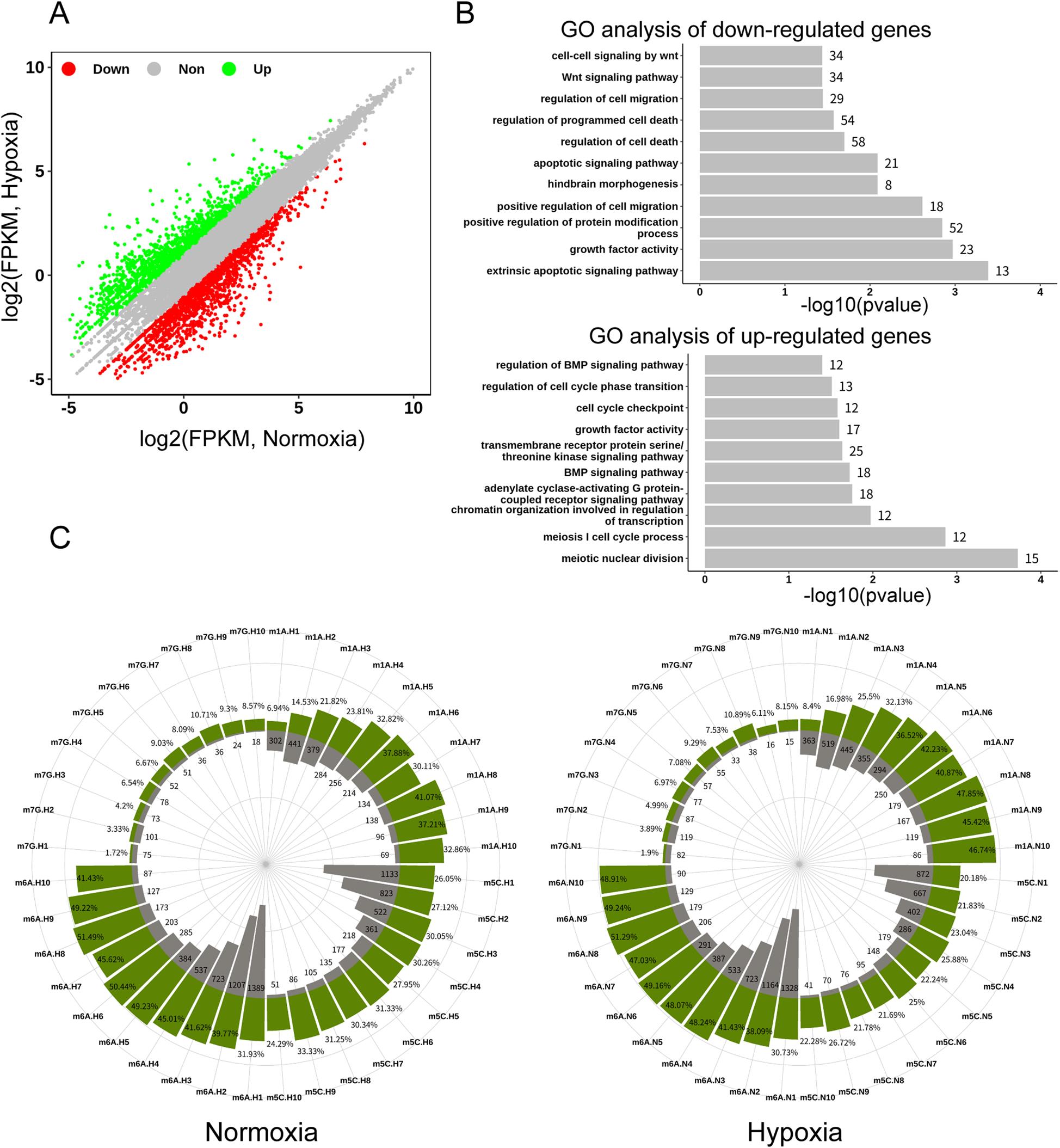
接下来,为了探究缺氧处理后RNA表达水平的变化,对脑组织样本进行了mRNA-seq。共鉴定出3087个差异表达基因。通过GO功能分析发现这些差异表达基因与斑马鱼大脑发育相关的后脑形态发生期显著相关。此外,作者还发现与轴突损伤相关的基因表达发生了改变,如Socs3a、Dpysl2b、Neurog1。提示脑损伤可能与缺氧诱导有关。
接下来,对RNA甲基化和RNA表达进行了关联分析。随着基因表达水平升高,这四种修饰的总体水平也逐渐升高。
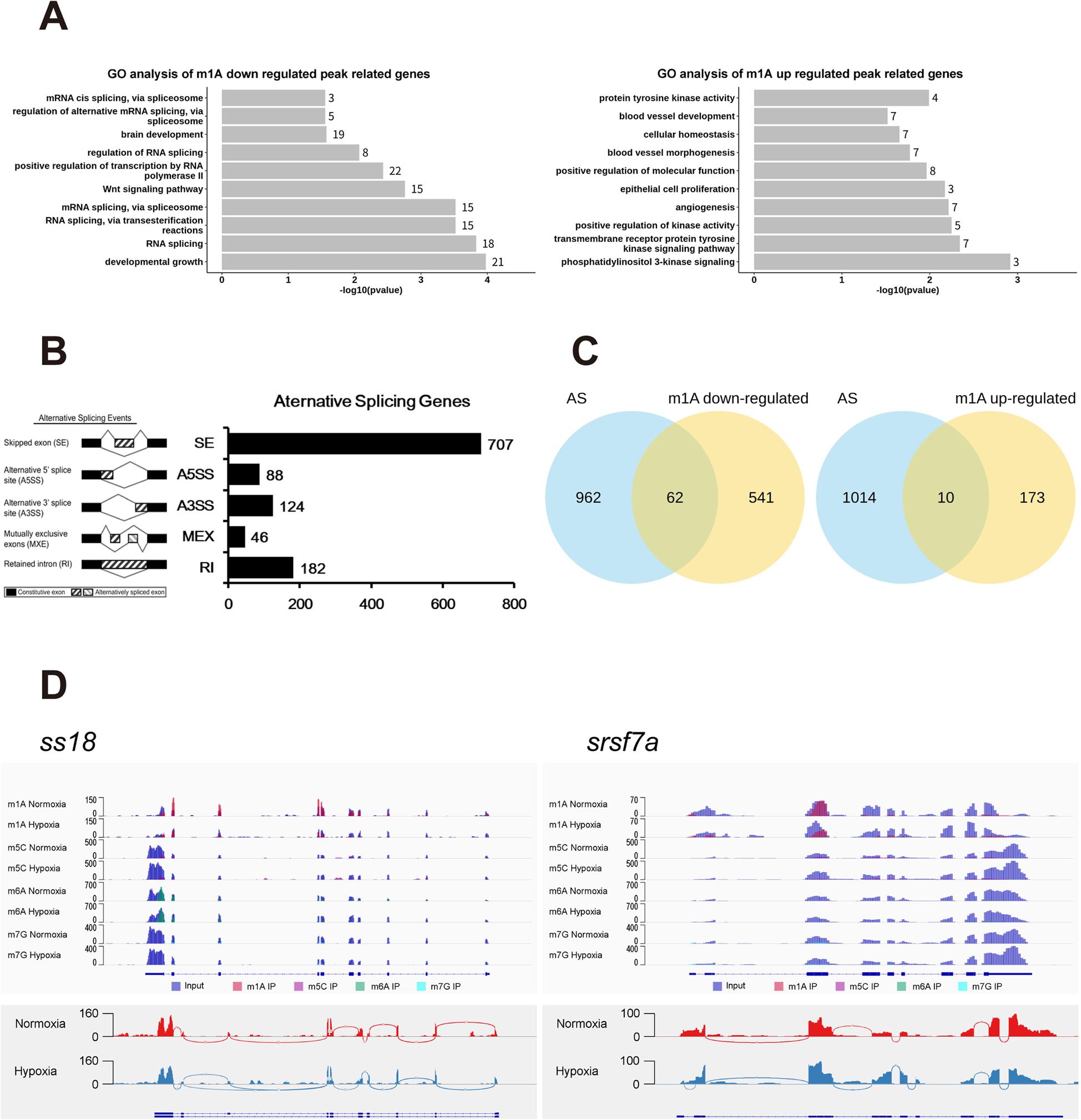
在斑马鱼脑组织中以m1A修饰最为丰富,根据m1A-MeRIP-seq测序结果对差异甲基化修饰的基因进行了GO富集分析。结果显示这些差异基因主要参与激酶活性、可变RNA剪接、Wnt信号通路等。一项研究指出,在人类基因组中,95%包含多个外显子的基因都具有选择性剪接(AS)。因此接下来探究了m1A对RNA剪接的影响,发现下调的m1A甲基化基因更有可能被AS靶向。其中转录激活因子ss18和剪接因子srsf7在缺氧组大脑中m1A修饰的丰度较低,这表明m1A修饰可能参与了AS。因此作者推测斑马鱼大脑可能通过改变m1A修饰水平来调节相关基因的表达进而应对缺氧诱导反应。
前面的结果显示四种修饰均在3’UTR占一定比例。此外,据报道哺乳动物大脑组织有丰富的miRNA,并且可能受m6A调控。因此,作者接下来分析斑马鱼脑组织中miRNA靶向的转录本是否更容易甲基化。结果表明, miRNA靶向的5个基因具有m1A、m5C、m6A和m7G甲基化修饰,其中m6A的丰度高于其他修饰。进一步探究显示miRNA靶选择的偏好与甲基化修饰有关。综上所述,mRNA的四种甲基化修饰可能与3’UTR区域的miRNA结合位点有关,其中m6A与miRNA的关系最为显著。
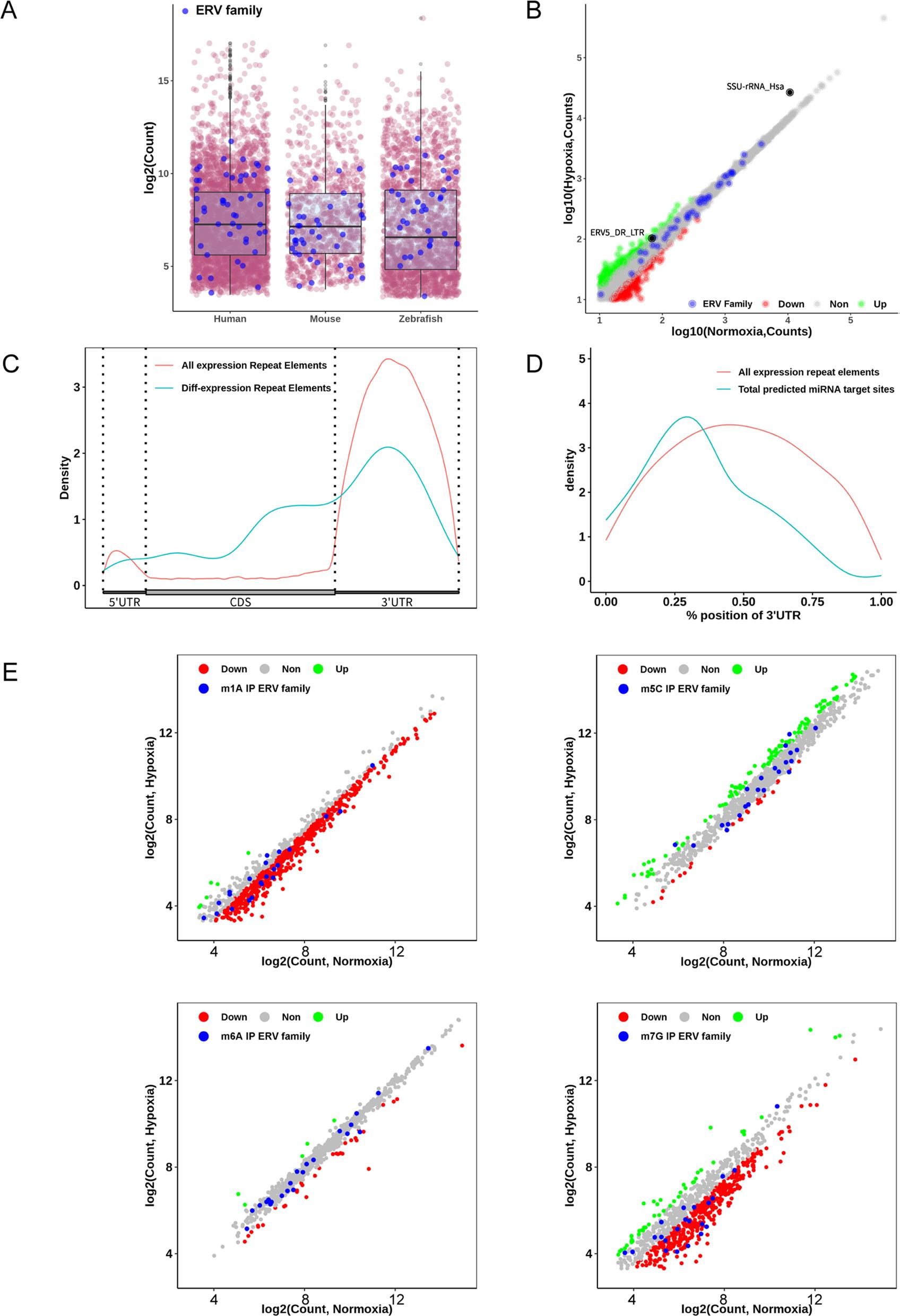
最近,有报道称miRNA来源于内源性逆转录病毒(ERV)和其他转座因子。前面的分析显示,miRNA在斑马鱼脑组织中的分布与RNA甲基化呈正相关。进一步分析发现,大多数ERV家族重复序列之间没有差异。接下来探究了斑马鱼脑转录本中重复元素(REs)的分布,发现REs主要富集在3’UTR区,与miRNA的分布也呈正相关。有研究表明, m6A通过转录后修饰调控ERVs的表达。结合测序数据,发现缺氧处理后,大多数REs的m1A和m7G甲基化水平下降,尤其是ERV家族。这些发现为今后研究脊椎动物脑组织中RNA甲基化修饰对ERV的调控提供了新的视角。
上海云序生物科技有限公司 商家主页
地 址: 上海市松江区莘砖公路518号24号楼4楼
联系人: 戴小姐
电 话: 021-64878766
传 真: 021-64878766
Email:market@cloud-seq.com.cn;liuqingqing@cloud-seq.com.cn
